“Linfoma” è il nome di un gruppo di tumori che prendono origine dal sistema linfatico. Non è una singola malattia ma un gruppo eterogeneo con caratteristiche epidemiologiche, istologiche, modalità di presentazione e approccio terapeutico. I due tipi principali sono il linfoma di Hodgkin (LH) ed il linfoma non Hodgkin (LNH). Nell’ultima classificazione della WHO (World Health Organization) del 2008 si annoverano 2 forme di LH e più di 40 tipi di LNH.
Il nostro Centro è membro della Fondazione Italiana Linfomi (FIL, www.filinf.it).
Epidemiologia
In base ai dati dell’AIRTUM (Associazione Italiana Registri Tumori) nel periodo 1998-2002 il linfoma di Hodgkin (LH) ha rappresentato lo 0,5% di tutti i tumori diagnosticati e ha causato lo 0,2% del totale dei decessi per cancro in entrambi i sessi. In media, ogni anno, vengono diagnosticati circa 4 casi ogni 100.000 uomini e 3 casi ogni 100.000 donne.
Il LH è raro nei bambini, ma rappresenta la neoplasia più comunemente diagnosticata negli adolescenti di età compresa tra i 15 ed i 19 anni. Nei Paesi occidentali si osservano due picchi di incidenza: con un primo nella popolazione di adolescenti e giovani adulti (tra i 15 e i 35 anni d’età) ed il secondo nei pazienti con più di 55 anni.
Eziologia
Al momento attuale le cause del LH non sono state ancora chiarite, ma si conoscono diversi fattori predisponenti, quali il virus di Epstein-Barr (EBV, lo stesso agente causale della mononucleosi), condizioni di disregolazione del sistema immunitario, come la presenza di malattie autoimmuni o stati di immunodeficienza, l’esposizione ad alcune sostanze tossiche. I dati epidemiologici relativi alla diversa incidenza della malattia in diverse regioni geografiche e le segnalazioni di famiglie con più membri affetti implicano l’associazione tra fattori ambientali e genetici nella patogenesi del LH.
Caratteristiche istologiche
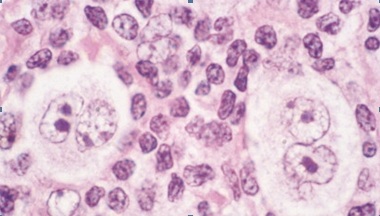
Secondo la classificazione WHO (World Health Organization) del 2008, il LH viene distinto nella forma classica (95% dei casi), a sua volta suddiviso nelle varietà a sclerosi nodulare, a cellularità mista, deplezione linfocitaria e ricca in linfociti, e la forma a predominanza linfocitaria nodulare (5% dei casi). La caratteristica morfologica peculiare del LH è la presenza delle cellule di Hodgkin e di Reed-Sternberg nella forma classica (Figura 1) e delle cellule lymphocyte-predominant (un tempo chiamate cellule istiocitiche-linfocitiche) nella forma a predominanza linfocitaria nodulare, nel contesto di un infiltrato infiammatorio di tipo reattivo (linfociti, neutrofili, eosinofili, monociti e macrofagi).
Manifestazioni cliniche
Nel 70-80% dei casi di LH la prima manifestazione clinica è una tumefazione linfonodale indolente nella regione del collo, in sede laterocervicale o sovraclaveare, senza sintomi di accompagnamento. Nel 60% dei casi si riscontra il coinvolgimento dei linfonodi del mediastino. Il mediastino è lo spazio toracico compreso tra le due cavità pleuriche ed è delimitato anteriormente dallo sterno, posteriormente dalla colonna vertebrale, lateralmente dalle pleure mediastiniche, superiormente comunica direttamente con le fasce cervicali attraverso uno spazio definito “stretto toracico superiore” ed inferiormente è delimitato dal diaframma. La presenza di una massa mediastinica può determinare sintomi compressivi, compromettendo le vie aeree, quali tosse stizzosa, dolore toracico, dispnea (“fame d’aria”), o sintomi correlati alla compressione dei vasi, ovvero la sindrome della vena cava superiore, caratterizzata da congestione ed edema del tessuti del capo, del collo, della parte superiore del torace e degli arti superiori (edema a mantellina), talvolta associata a trombosi venosa. Dalla sede iniziale la malattia tende a diffondersi in senso assiale, interessando per contiguità le sedi linfonodali vicine. La diffusione ad organi extra-linfatici (scheletro, polmone, fegato), molto rara all’esordio ma più frequente negli stadi più avanzati, avviene per estensione diretta della massa linfonodale o per disseminazione attraverso il sangue.
Circa il 40% dei pazienti presenta alla diagnosi sintomi sistemici definiti “sintomi B”, quali febbre intermittente, sudorazioni profuse, soprattutto notturne e perdita di peso (non secondaria a diete). Altri sintomi sono il prurito generalizzato (talora di notevole entità), la spossatezza e il dolore in sede di localizzazione linfonodale di malattia scatenato dall’assunzione di alcol, che compare in meno del 10% dei pazienti.
Diagnosi, stadiazione e definizione dei fattori prognostici
Per la diagnosi iniziale di LH è essenziale eseguire una biopsia escissionale di un linfonodo o di una sede extra-linfonodale sospetti per localizzazione di malattia.
Per “stadiazione” si intende la valutazione dell’estensione della malattia. Le metodiche strumentali utilizzate sono la radiografia del torace, la TC del collo-torace-addome (tomografia computerizzata) con mezzo di contrasto, la PET/TC (tomografia ad emissione di positroni combinata con la TC) e la biopsia osteomidollare. Queste indagini permettono di definire lo stadio della malattia, secondo il sistema di stadiazione di Ann Arbor, che prevede uno STADIO I in caso di interessamento di un solo linfonodo o di una sola stazione linfonodale; uno STADIO II in caso di interessamento di due o più stazioni linfonodali, tutte al di sopra o sotto il diaframma; STADIO III in caso di interessamento di stazioni linfonodali sia sopra che sotto il diaframma; STADIO IV in caso di interessamento di strutture extra-linfatiche (Figura 2).
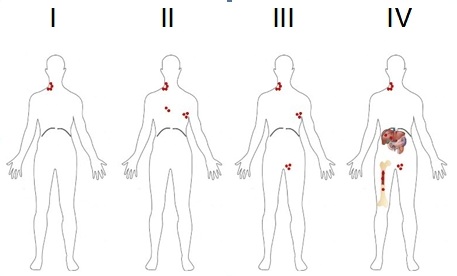
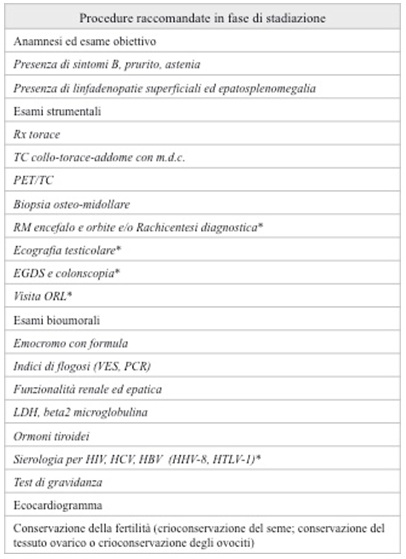
In base alla presenza dei sintomi B lo stadio viene ulteriormente distinto in A (assenza dei sintomi) o B (presenza dei sintomi). Il termine Bulky viene usato per identificare una massa tumorale di grandi dimensioni (linfonodali superiori ai 10 cm o allargamento mediastinico maggiore di un terzo del diametro toracico). Gli stadi I e II vengono definiti stadi iniziali, mentre il III e IV sono gli stadi avanzati. Alla diagnosi vengono inoltre eseguite altre indagini volte a indagare la funzionalità d’organo, quali esami ematochimici e sierologici (emocromo con formula, funzionalità epatica e renale, indici di flogosi quali VES e PCR, profilo proteico, LDH e b2microglobulina, test di gravidanza nelle donne in età fertile); elettrocardiogramma ed ecocardiogramma e prove di funzionalità respiratoria (spirometria). Prima di iniziare la chemioterapia, se le condizioni cliniche lo permettono, viene offerta la possibilità di eseguire la conservazione della fertilità (crioconservazione del seme; conservazione del tessuto ovarico o crioconservazione degli ovociti) (Tabella 1).
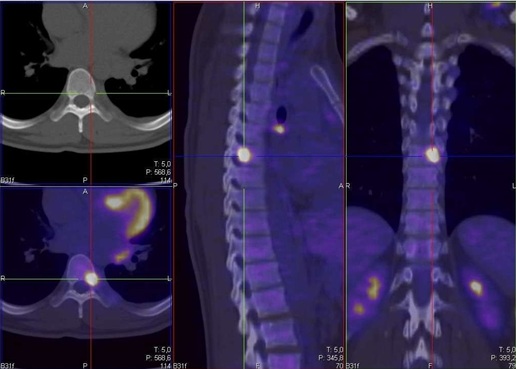
I principali fattori prognostici sfavorevoli del LH sono, negli stadi iniziali, l’età superiore a 50 anni, la VES (superiore a 50 mm/h alla diagnosi), la presenza di sintomi B, la presenza di masse bulky, coinvolgimento di più di 3 regioni linfonodali; mentre, negli stadi avanzati, sono considerati fattori sfavorevoli l’età superiore a 45 anni, la leucocitosi (globuli bianchi superiori a 15.000/mL), la linfopenia (linfociti inferiori a 600/mL o all’8% dei leucociti totali), l’anemia (emoglobina inferiore a 105 g/L), albumina < 40 g/L, sesso maschile, ed il coinvolgimento di sedi extra-nodali alla diagnosi. Recenti studi hanno dimostrato inoltre come il risultato della PET/TC, eseguita precocemente durante la terapia, abbia un forte potere predittivo sull’andamento della malattia (Figura 3).
Terapia
Negli ultimi 20 anni l’appropriato utilizzo degli schemi di chemioterapia, talora in associazione alla radioterapia, ha permesso di ottenere elevate percentuali di remissioni, sia negli stati iniziali che in quelli avanzati di malattia. Gli studi clinici eseguiti hanno consentito di abbandonare terapie gravate da elevata tossicità a breve e lungo termine (come, ad esempio, lo schema MOPP), prediligendo terapie meno tossiche ma di pari efficacia. Il trattamento standard che viene attualmente utilizzato è lo schema ABVD, costituito da 4 farmaci (Adriamicina, Bleomicina, Vinblastina e Dacarbazina) che vengono somministrati tramite infusione endovenosa (in una vena periferica o, preferibilmente, in una vena centrale tramite l’inserzione di un catetere venoso). Ciascun ciclo viene somministrato ogni 28 giorni (4 settimane); esso consiste in 2 somministrazioni a distanza di 15 giorni (2 settimane) (dal punto di vista pratico il paziente viene sottoposto a chemioterapia ogni 2 settimane). Negli stadi avanzati un’alternativa è lo schema BEACOPP escalated o baseline (Bleomicina, Etoposide, Adriamicina, Ciclofosfamide, Vincristina, Procarbazina, Prednisone), che permette di ottenere delle percentuali di risposta superiori ma è gravato da notevole tossicità, a breve e a lungo termine. Il numero di cicli e l’eventuale radioterapia sulle sedi coinvolte (involved-field) dipende dallo stadio della malattia alla diagnosi e dai fattori di rischio presenti: nei casi più favorevoli è possibile un programma di chemioterapia abbreviato, costituito da 2 cicli secondo schema ABVD, seguiti da radioterapia; fino ai 6 cicli degli stadi avanzati. Gli effetti collaterali più frequenti sono la nausea ed il vomito; l’effetto tossico sul midollo osseo, che si manifesta con una riduzione dei globuli bianchi (in particolare dei neutrofili); l’alopecia (ovvero la caduta dei capelli e dei peli) per l’effetto sui bulbi piliferi ed, infine, la spossatezza. Altri effetti di più rara insorgenza sono la comparsa di formicolii alle dita delle mani e dei piedi (segno di neurotossicità dovuta alla vinblastina), la cardiotossicità (dovuta all’adriamicina) che può portare a gravi quadri di cardiomiopatia fino allo scompenso cardiaco; la tossicità polmonare (bleomicina, specie se associata alla radioterapia); lo sviluppo di secondi tumori, sia ematologici che extra-ematologici.
Circa il 15-20% dei pazienti con stadio iniziale ed il 35-40% degli stadi avanzati non ottengono la remissione con la terapia di prima linea o manifestano una recidiva dopo il raggiungimento della remissione. La chemioterapia di salvataggio utilizzata consiste negli schemi IEV (Ifosfamide, Etoposide, Epirubicina), IGEV (Ifosfamide, Gemcitabina, Vinorelbina) o DHAP (Cisplatino, Citarabina ad alte dosi, Desametasone) con raccolta delle cellule staminali e successivo trapianto autologo. Per i pazienti che presentano una ricaduta di malattia dopo trapianto autologo di cellule staminali ematopoietiche, vengono utilizzati nuovi farmaci, come la bendamustina ed il brentuximab vedotin, seguiti da trapianto allogenico (da donatore familiare o da registro).
Numerosi sono gli studi clinici in corso (in Italia e all’estero) che stanno testando nuovi farmaci (inibitori delle iston-deacetilasi, inibitori di mTOR, immunomodulanti, etc) da soli o in associazione a protocolli standard di terapia, sia in prima linea che nei casi refrattari o in recidiva.
Studi in corso
Presso il nostro Centro sono attivi i seguenti studi multicentrici:
- Studio GITIL-HD0607: ”Multicentre clinical study with early treatment intensification in patients with high-risk hodgkin lymphoma, identified as FDG-PET scan positive after two conventional ABVD courses”. Sponsor: Gruppo Italiano Terapie Innovative nei Linfomi (G.I.T.I.L.)
- Studio FM-HD09-01: “Phase III study comparing Rituximab-supplemented ABVD (R-ABVD) with ABVD followed by involved-field radiotherapy (ABVD-RT) in LIMITED-stage (STAGE I-IIA WITH NO AREAS OF BULK) Hodgkin’s lymphoma”. Sponsor: Fondazione Michelangelo.
- Studio 2P-HD10: ”Interim PET con studio di acquisizione a due tempi (2P-PET) effettuata dopo 2 cicli di chemioterapia con ABVD nel Linfoma di Hodgkin in stadio limitato con lesioni linfonodali “bulky” – 2P-HD10”. Sponsor dello studio: Fondazione Italiana Linfomi (FIL).

